
时间:2022-05-06 16:00:37来源:网络整理
作者:济宁医学院临床学院(李雪松,元龙);济宁医学院附属医院(孟春阳)
目前对神经性疼痛的治疗只能缓解症状,但不能缓解潜在的疼痛。几十年来,疼痛研究一直围绕着氧化-硝化应激、蛋白激酶和炎症反应信号级联,但没有一个针对神经性疼痛产生特异性和有效的治疗方法。近来,鸟苷三磷酸环水解酶1(GTPcyclohydrolase1,GCH1)和四氢生物蝶呤,BH4)通路成为神经性疼痛研究的焦点,因为参与BH4合成的通路限速酶GCH1已被发现可以减轻神经性疼痛。Tegeder 等人发现 GCH1 是周围神经性疼痛和炎症性疼痛的关键调节因子。GCH1 和 BH4 是神经性疼痛过程中的重要参与者。 BH4与神经性疼痛共同探索神经性疼痛的机制,寻找新的治疗靶点。
1.GCH1
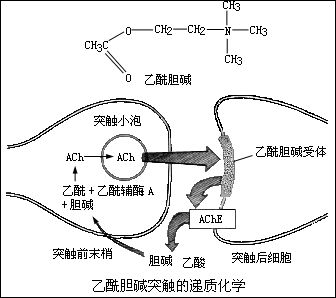
GCH1基因是国际公认的与疼痛发生密切相关的众多基因之一。 GCH1基因位于14q22.1~q22.2,在基因组DNA上跨越约60.8kb,由6个外显子和2个内含子组成。编码 750 个氨基酸。 GCH1是BH4合成中最重要的限速酶,GCH1活性的降低导致BH4的产生减少。此外,GCH1被发现是周围神经性和炎症性疼痛的主要调节因子,GCH1基因突变可能会降低疼痛敏感性。
2006 年,Tegeder 等人。首次阐明了GCH1基因与疼痛的关系。当周围神经受损或炎症时,GCH1活性增强,背根神经节(DRGs)中BH4表达增加。发现在大鼠疼痛模型中腹腔注射 GCH1 合成抑制剂 2,4-二氨基-6-羟基嘧啶 (DAHP) 可显着改善大鼠的神经性疼痛症状。此外,将构建的靶向GCH1短发夹RNA(rAAV-shGCH1)的重组腺相关病毒在神经性疼痛大鼠模型的坐骨神经周围注射,发现rAAV-shGCH1可以有效沉默GCH1,它还具有减轻疼痛的作用。
泰格德等人。研究了椎间盘突出症后的患者,发现GCH1基因单倍型的疼痛缓解明显优于普通人群。 Campbell 等人的结果。表明 GCH1 基因的单核苷酸多态性显着影响疼痛评分。多林等人。在疼痛诊所的患者中发现,正常人群所需的镇痛药量显着高于 GCH1 基因单倍型人群。 Lötsch 等人的结果。研究表明,与正常人相比,GCH1基因单倍型的癌症患者使用少量吗啡可以达到更好的镇痛效果和更低的疼痛评分。此外,GCH1 基因单倍型也在相关疼痛中起作用。本课题组前期研究发现,大鼠脊髓背角次级神经元中GCH1水平也随着疼痛的加重而发生动态变化,证实了GCH1的表达与神经性疼痛密切相关。
综合分析表明,GCH1基因表达增加可增加BH4的合成,从而促进疼痛敏感物质的合成和释放,这可能是神经性疼痛的机制。然而,由于遗传和表型的多样性,其分子机制尚不清楚。继续研究GCH1基因在神经病理性疼痛中的作用机制是我们未来的研究方向。
2.BH4
1)BH4合成:BH4是一种芳香族氨基酸羟化酶[如苯丙氨酸羟化酶(PAH)、酪氨酸羟化酶(TH)和羟化酶(TPH)]也是三种一氧化氮合酶(NOS)的辅酶) [内皮一氧化氮合酶 (eNOS)、诱导型一氧化氮合酶 (iNOS) 和神经元一氧化氮合酶 (nNOS)] 是重要的辅助因子。因此,BH4可能存在于高等生物的每一个细胞或组织中,并在一些神经递质的形成、免疫反应和敏感性相关的生物学过程和病理状态中起关键作用。
BH4的合成有3条途径:新生途径、补救途径和再循环途径。从头合成途径是BH4合成最重要的途径。三磷酸鸟苷 (GTP) 由 GCH1 催化形成 7,8-三氢蝶呤,随后由 6-丙酮四氢蝶呤合酶 (PTPS) 转化。它是6-丙酮酰四氢蝶呤(PTP),在mupterin还原酶(SPR)的作用下最终还原为BH4。补救途径是利用从头合成途径的中间产物6-丙酮酰四氢蝶呤在醛糖还原酶(AR)或羰基还原酶(CR)的作用下生成6-丙酰四氢蝶呤,再转化为6-丙酰四氢蝶呤。它在独立酶的作用下参与分子基团的重排生成moterin(SP),在SPR或CR的作用下转化为7,8-二氢生物蝶呤(BH2)),并进一步还原通过二氢叶酸还原酶 (DHFR) 生成 BH4。
当合成的BH4作为芳香族氨基酸羟化酶的辅酶反应时,BH4上的单分子氧被转移到相应的氨基酸上,BH4被氧化成BH4-4α-甲醇胺。 BH4-4α-甲醇胺可通过蝶呤-4α-甲醇胺脱氢酶(PCD)还原为喹啉二氢蝶呤(qBH2)),然后在体内被喹啉二氢蝶呤还原酶还原为BH4,完成循环合成途径。
2)BH4与神经性疼痛:正常情况下,机体对BH4合成有严格细致的生理调节,但受损病理系统BH4水平升高。 BH4 是产生酪氨酸、多巴胺、去甲肾上腺素和一氧化氮的重要辅助因子。过多的 BH4 水平会引起疼痛,并且可能与这些过量的神经递质或信号分子的产生有关,尤其是在背根神经节中。 BH4 水平的上调在疼痛信号传导中起关键作用。当机体处于正常基础状态时,BH4的从头合成途径表现出低活性。虽然BH4的水平比较低,但仍处于正常生理范围内。此时的补救合成途径在维持体内足够的 BH4 水平方面发挥着重要作用。效果。
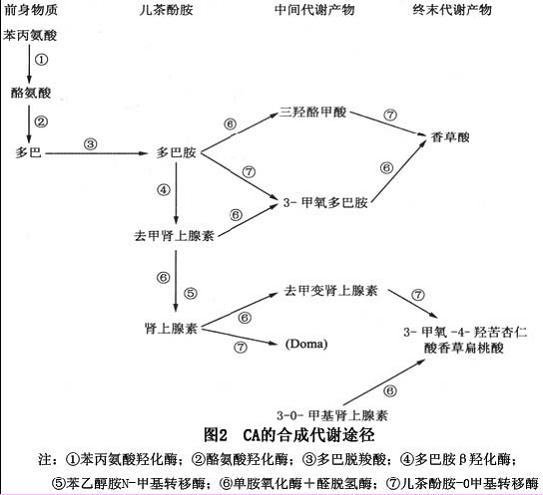
周围神经损伤后,随着GCH1表达上调,原代感觉神经元BH4表达也升高,SPR和喹诺二氢生物蝶呤还原酶水平升高,虽然变化不大,但可导致原发性感觉神经元明显升高。 BH4 水平。在慢性炎症状态下,BH4合成所需的酶水平没有增加,但酶的活性显着增加。由于酶活性的增加,在背根神经节中产生了过量的 BH4。在BH4的作用下,NOS接受还原型磷酸二核苷酸(NADPH)的电子,还原分子氧并氧化L-,NOS将电子传递给L-精氨酸被氧化成L-瓜氨酸,催化生成一氧化氮(NO) .
研究表明,BH4 诱导的疼痛行为是由 NO 产生介导的。 NO 是一种自由基,是第一个被发现参与细胞信号传导的气体信号分子。 NO参与各种生命活动,其在人体内的合成严格受制于BH4的参与。研究结果表明,腹腔注射NO前体或NO供体可增强神经性疼痛大鼠的热痛感和异常性疼痛;注射NOS抑制剂可有效改善脊髓神经损伤大鼠的触觉异常性疼痛;使用基因敲除小鼠,证明在足底注射或完全弗氏佐剂 (CFA) 或 5% 诱导的疼痛模型中,与野生型小鼠相比,NOS-/- 小鼠的疼痛减轻了,在神经性疼痛模型中,NOS-/-小鼠的神经损伤引起的行为减少。
Latremoliere 等人。表明未受伤的背根神经节神经元中 BH4 合成增加足以诱导热痛敏感性鸟苷酸环化酶 信号通路,并且这种作用的具体机制可能是通过增加 NO 合成。此外,BH4 也可能直接参与疼痛的产生。纳赛尔等人。将 BH4 注射到大鼠脚底鸟苷酸环化酶 信号通路,以研究 BH4 是否可以通过周围神经起作用。研究人员发现BH4作用于周围神经也会引起疼痛,而BH4引起的疼痛可能与NO和前列腺素无关。这表明BH4很可能通过未知途径或直接介导疼痛的发生,具体机制有待进一步研究。
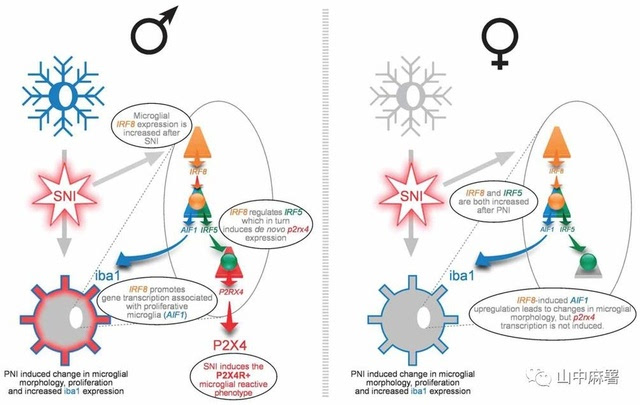
抑制 BH4 的异常合成可防止 NO 引起的背根神经节过度神经损伤,从而减轻神经性和炎症性疼痛。奇德利等人。发现它是一种有效的 SPR 抑制剂。 SPR是BH4合成的第三个限速酶,其表达水平在神经损伤时上调。抑制 SPR 会降低 BH4 水平,导致 BH4 水平降低,从而产生镇痛作用,而对中枢和周围神经系统没有严重的不良影响。
综上所述,GCH1 和 BH4 确实与神经性疼痛的发展相关,沉默 GCH1 以阻断神经系统中 BH4 合成途径的治疗策略应将 BH4 降低至非病理水平,从而产生镇痛作用。然而,它们相互作用的分子机制仍然缺乏。因此,我们以此为切入点,进一步研究神经性疼痛的相关分子机制,进而为靶向GCH1和BH4治疗神经性疼痛提供理论依据和新思路。
资料来源:李雪松、元龙、孟春阳。三磷酸鸟苷环化水解酶1和四氢生物蝶呤与神经性疼痛的研究进展[J].中国医师进步杂志, 2018, (9)@ >:844-847.
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐

2022-05-06 15:58:03

2022-05-06 15:01:40

2022-05-06 14:58:03

2022-05-06 10:58:03
2022-05-06 09:05:37

2022-05-06 08:58:03
热点排行
精彩文章

2022-05-06 15:58:05

2022-05-06 14:58:06

2022-05-06 12:58:05

2022-05-06 11:58:04
2022-05-06 11:06:16

2022-05-06 09:58:07
热门推荐
