
时间:2022-07-22 18:00:32来源:网络整理
编号:G633.8 文献编号:C 氨气催化氧化是高中化学教学中的一项重要实验,对氨气性质的教学和氨气的工业化生产具有十分重要的意义。硝酸。学过这个实验的老师都会发现,这个实验也是高中化学比较难的实验之一。本实验的成功与否受几个实验条件的控制,如原料气中氧氨的比例、水蒸气的影响、催化剂的制备、催化温度的控制等。本文将再次研究实验成败的关键,并对实验装置进行一些改进。 1.1 吹风速度的影响是氨催化氧化的经典实验装置示意图,不仅在高中课本中经常出现,在无机化学或普通化学的大学课本中也经常出现。本实验的很多操作说明或者类似的实验研究文章都会提到吹气速度的控制,即通过控制吹气的速度来达到合理的氨氧比,但是笔者查阅了很多资料。后来发现没有详细说明如何控制所谓的“吹气速度”。通常我们会理解为起泡速度过快导致浓氨水带出过多或NO2反应生成含有硝酸铵或亚硝酸铵的白烟市售氨水浓度,但实际上大多数实验失败时也会出现类似的情况;如果吹气速度太慢,带出的氨气量太少,达不到反应所需的浓度,不仅不能使催化剂保持红热状态,而且不利于NO2 的产生。通过多次实验,作者对这种不明确的“充气速度”产生了怀疑。

图2所示的实验装置旨在对吹气速度进行初步研究。实验数据见表1。 分别取质量分数约为21%的浓氨水进行上述实验,以每分钟打气球多少次来比较吹气速度,用500mL量筒测量排出水的体积。四个实验均在相同条件下进行,唯一的变量是吹气速度。从实验数据不难看出,虽然吹气速度不同,差异较大,但单位体积空气所能带出的氨气量基本不变。显然,在一定的温度和压力下,一定浓度的氨水的挥发性是恒定的。这个实验终于证明了一个简单的常识。氨水的挥发性,即氨水的饱和蒸气压,只与温度、浓度和压力有关。虽然只是初步实验,但“氨催化氧化”实验的成败显然与吹气速度没有直接关系。当然,很容易理解,极快或极慢的放气也会对实验产生不利影响。 1.2 浓度的影响 排除了“风速”对实验可能产生的影响后,我们再来看看浓度。为保证实验的成功,氨水的浓度要适当。查阅相关资料后发现,有人用11%的氨水,也有人按照这些比例用21%做实验。结果并不能保证每次都成功。我相信其他老师也有类似的经历。主要原因是每次实验的室温不同,造成氨水的温度不同,其饱和蒸汽压发生变化,所以氨水的浓度要根据室温来调整。
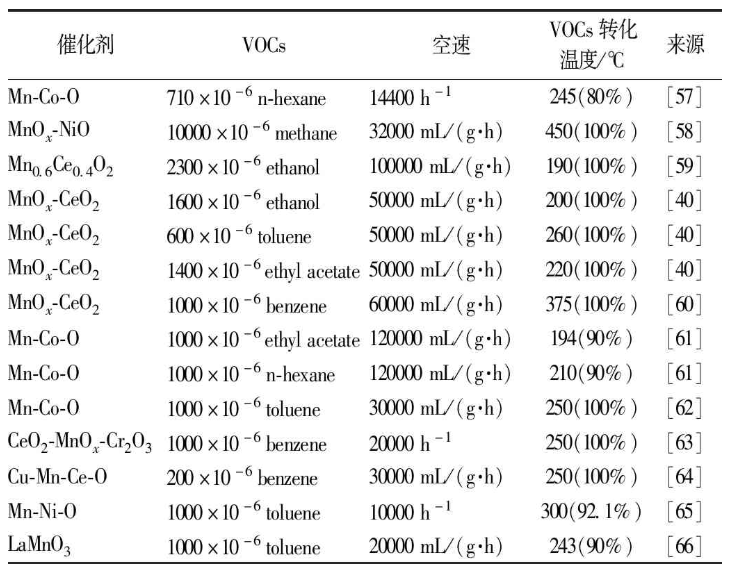
市售浓氨水的质量分数约为27%,20时的密度为0.9 gmL-1。笔者通过实验发现,当氨浓度接近以下关系时,实验可以取得满意的结果。具体制备方法见表2。 1.3催化剂和催化温度的影响 很多老师在做这个实验时使用市售的三氧化铬作为催化剂市售氨水浓度,发现催化效果不好,很难达到炙手可热的状态。三氧化铬还有其他问题吗?笔者对比了几种常见的过渡金属氧化物催化剂,发现三氧化铬的催化效果最为理想,与教科书中的说法一致。但是市售的三氧化铬的催化效果确实差强人意,而采用热分解重铬酸铵的方法制备的催化剂活性较好,可能是因为这种方法制备的三氧化铬非常松散,存在较大的原因接触面积。这种方法制备的三氧化铬可以重复使用,只要在储存时注意干燥,每次使用前在石棉网上加热干燥即可再次使用。选择这种催化剂的另一个好处是很容易观察到催化剂的红热现象,这也是本实验中最重要的实验现象之一。这种现象的出现表明氨催化氧化的大部分实验已经成功。那么当气体膨胀时,催化剂的红热在什么温度下最有可能出现呢?笔者做了很多实验,发现当催化剂的颜色受热,其绿色开始变深时,气体膨胀时最容易出现红热。 , 去除酒精灯后催化剂仍保持红热状态。
以上问题解决后,可以看到烧瓶内缓慢产生红棕色二氧化氮气体,但同时烧瓶内大量水蒸气凝结,使烧瓶内呈红棕色看起来模糊。这主要是因为氨气氧化后会产生大量的水。水蒸气的存在不仅不利于二氧化氮的观察,还会吸收二氧化氮形成硝酸雾。因此,可以对原装置进行如图所示的改进,在燃烧管和烧瓶中加入装有无水氯化钙的干燥管。这里的氯化钙不仅有干燥作用,还能吸收多余的氨气,可以更直接清晰地观察到红棕色的二氧化氮气体。 [1] 刘光启,马连祥,刘杰主编。 《化学化学性质资料手册(无机卷)》[M].化学工业出版社,2002.

声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐
2022-07-22 13:01:16
2022-07-22 11:01:49
2022-07-22 10:02:02
2022-07-22 09:02:51
2022-07-21 18:03:21

2022-07-21 17:02:27
热点排行
精彩文章

2022-07-22 14:01:41
2022-07-22 12:02:08

2022-07-22 09:02:42

2022-07-22 09:02:25

2022-07-21 18:03:49
2022-07-21 17:02:40
热门推荐
